Bei Applus+ Laboratories bieten wir Ihnen unsere hervorragenden Prüfleistungen für Medizinprodukte an. Diese helfen Ihnen dabei, die Entwicklung und die Konformitätsbewertung Ihrer Medizinprodukte und deren Biokompatibilität hinsichtlich regulatorischer Vorgaben zu verbessern und gleichzeitig die Sicherheit Ihrer Produkte zu gewährleisten. Die Biokompatibilitätsprüfung ist Teil unserer anderen Chargenfreigabe-Prüfleistungen:
- Validierung der Reinigung
- Validierung der Verpackung
- Validierung der Stabilität
- Material- und chemische Charakterisierung
Warum ist die Biokompatibilitätsprüfung für Medizinprodukte wichtig?
Die Biokompatibilitätsprüfung für Medizinprodukte ist unerlässlich, um sicherzustellen, dass jedes Material, jede Komponente oder jedes fertige Produkt, das mit dem menschlichen Körper in Kontakt kommt, keine schädlichen biologischen Reaktionen auslöst. Durch die Biokompatibilitätsprüfung von Medizinprodukten können Hersteller bewerten, ob ein Produkt sicher, chemisch stabil und für seinen vorgesehenen klinischen Einsatz geeignet ist. Dieser Prozess ist auch zentral für den Nachweis der regulatorischen Konformität, da globale Behörden eine umfassende biologische Bewertung als Teil der Produktzulassung verlangen.
Biokompatibilitätsprüfungen für Medizinprodukte bewerten die Wechselwirkungen zwischen Produktmaterialien und biologischen Systemen und stellen sicher, dass das Produkt keine zytotoxischen, reizenden, sensibilisierenden oder systemisch toxischen Wirkungen hervorruft. Diese Bewertungen bilden eine grundlegende Komponente des Risikomanagements und der Patientensicherheit.
Die chemische Charakterisierung umfasst mehrere Teile der Norm ISO 10993:
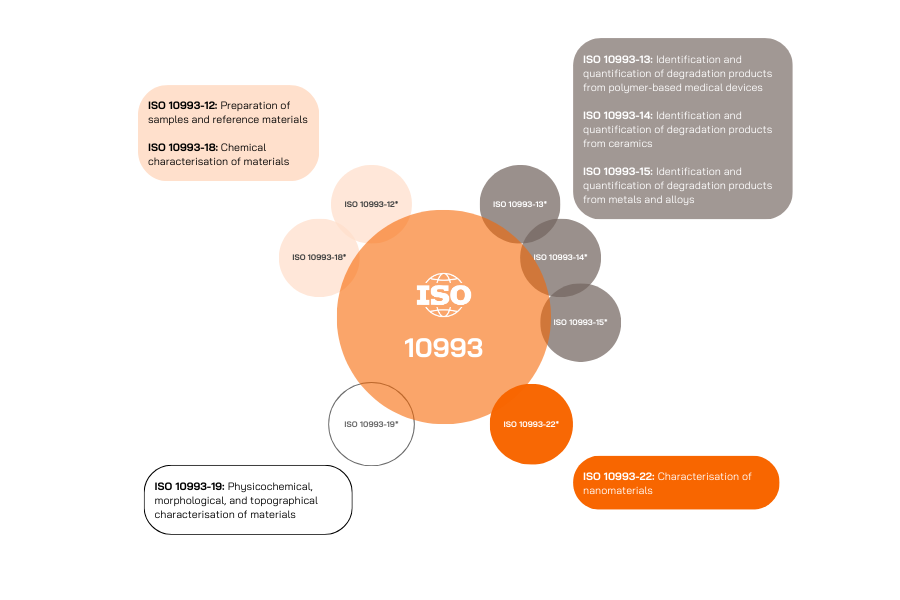
Leitlinien zur Durchführung der Biokompatibilitätsbewertung sind in ISO 10993-1 enthalten und geben die erforderlichen Prüfungen entsprechend dem Produkttyp, der Kontaktdauer und der Art des Körperkontakts vor.
Besondere Aufmerksamkeit ist dem Potenzial des Materials zu widmen, Verbindungen freizusetzen (im Zusammenhang mit dem Herstellungsprozess oder dem Materialabbau im Anfangsstadium und nach Alterung), um das Verfallsdatum zu validieren.
Chemische Charakterisierung und Extractables- und Leachables-Prüfung
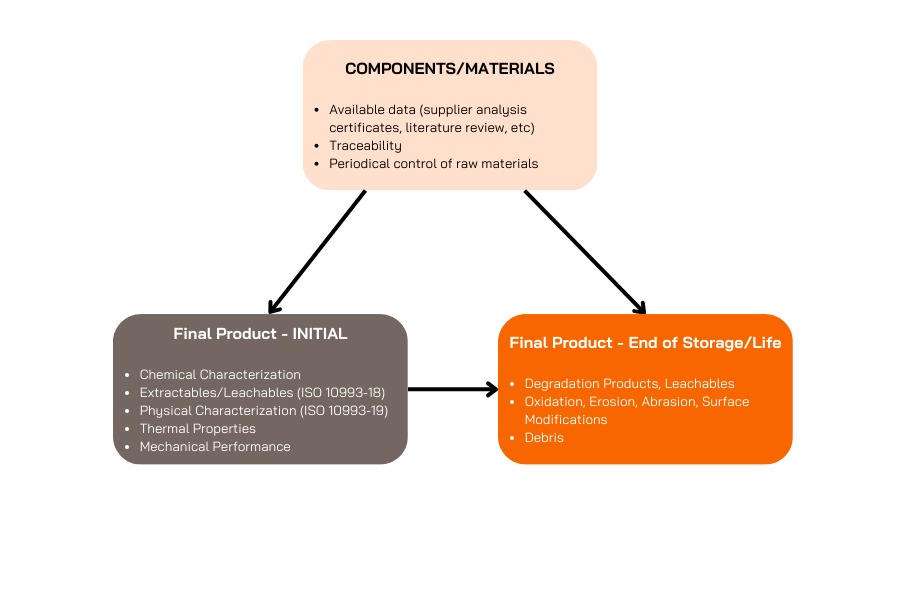
Die Charakterisierung des Materials in seiner Anfangsphase ist wichtig, um das Risikoniveau zu bestimmen und die Freisetzung chemischer Verbindungen oder unkontrollierter Produkte zu identifizieren, die die Gesamtsicherheit der Produkte beeinträchtigen könnten. Diese Charakterisierung ist der allererste Schritt bei der Ausarbeitung der biologischen Bewertungsstrategie und der Anforderungen.
Die Bestimmung der chemischen Charakterisierung nach Alterung sowie der Wechselwirkung des Medizinprodukts mit seiner Verpackung ist ebenso wichtig, um die Haltbarkeit festzulegen und das Verfallsdatum zu bestimmen.
Physikochemische Analysen gemäß ISO 10993-12 und ISO 10993-18
Diese erste Analyse konzentriert sich auf die Untersuchung der physikalischen und chemischen Eigenschaften der Materialien, die in Medizinprodukten verwendet werden.
Alle Proben von Medizinprodukten werden gemäß den Anforderungen der ISO 10993-12 extrahiert (abhängig von der Art des Kontakts, der Dauer, dem Zielmarkt und der chemischen Beschaffenheit des Produkts).
Die Norm ISO 10993-18 gibt Leitlinien zur Identifizierung und Quantifizierung chemischer Substanzen, die potenziell aus dem Material des Medizinprodukts freigesetzt werden könnten, einschließlich extrahierbarer und auslaugbarer Stoffe, der chemischen Zusammensetzung des Materials und seiner chemischen Struktur.
- Analyse flüchtiger Verbindungen (VOC) wie Restlösungsmittel (terpenoid) und Alkohole mittels Headspace-Gaschromatographie (HS-GC-MS)
- Analyse halbflüchtiger Verbindungen (SVOC) wie Restmonomere und niedermolekulare Additive (Alkane, Alkohole, Ester, Siloxane…) mittels Gaschromatographie (GC-MS)
- Analyse nichtflüchtiger Verbindungen (NVOC) wie Herstellungs- und Materialadditive (hochmolekulare Additive) mittels Flüssigchromatographie (LC-MS)
- Analyse mineralischer und anorganischer Verbindungen mittels ICP-OES und ICP-MS
- Analyse ionischer Verbindungen (Phosphat, Chlorat, Nitrat, Bromid,…) mittels Ionenchromatographie (IC)
Physikochemische, morphologische und topografische Charakterisierung von Materialien gemäß ISO 10993-19
Zusätzlich zu diesen verpflichtenden Bewertungen können weitere chemische Charakterisierungen durchgeführt werden, um Ihre Medizinprodukte besser zu charakterisieren (FTIR, SEM, DSC, SEC). Mehr Details zur chemischen Charakterisierung.
Ein wesentlicher Bestandteil der biologischen Bewertung von Medizinprodukten ist dieser Prozess, der eine umfassende Analyse der physikalischen, chemischen und Oberflächeneigenschaften der in Medizinprodukten verwendeten Materialien umfasst, um deren Sicherheit, Leistung und Biokompatibilität zu gewährleisten. Das Verständnis dieser Eigenschaften hilft Ihnen vorherzusagen, wie das Material mit biologischen Systemen interagieren wird.
Die Norm ISO 10993-19 deckt viele verschiedene Aspekte ab, von der Analyse der elementaren und molekularen Zusammensetzung von Materialien über deren thermische Eigenschaften bis hin zur Oberflächenstruktur und Morphologie sowie der Oberflächenbenetzbarkeit und Hydrophobie.
Analyse von Abbauprodukten (ISO 10993-13/14/15)
Ein weiterer entscheidender Aspekt ist die Kontrolle der Entwicklung des Produkts im Laufe der Zeit.
Unkontrollierte Abbauprodukte und Herstellungsnebenprodukte müssen letztlich überprüft werden, um die langfristige Sicherheit der Produkte sowohl unter Lagerbedingungen als auch unter Einsatzbedingungen im Körper zu gewährleisten
Durch diesen Prozess können wir die Langzeitstabilität und Sicherheit polymerbasierter Medizinprodukte verstehen, indem wir alle Nebenprodukte identifizieren und quantifizieren, die beim Abbau des Materials im Laufe der Zeit freigesetzt werden.
In diesem Teil der Biokompatibilität werden Stabilitätsprüfungen durchgeführt und ähnliche Tests wie nach ISO 10993-18 nach Alterung durchgeführt. Bei metallischen Implantaten können Korrosionsbeständigkeit und Metallfreisetzung bewertet werden.
Unterstützung bei der regulatorischen Konformität für Biokompatibilitätsprüfungen von Medizinprodukten
Der Nachweis der Einhaltung internationaler Vorschriften ist ein entscheidender Bestandteil der Biokompatibilitätsprüfung von Medizinprodukten. Regulierungsbehörden wie die FDA (Vereinigte Staaten), die MDR (Europäische Union) und andere globale Institutionen verlangen eine umfassende biologische Bewertung gemäß ISO 10993-1. Die Anforderungen an die Biokompatibilitätsprüfung für Medizinprodukte umfassen die Risikobewertung, die Auswahl geeigneter biologischer Tests, die Begründung von Testausnahmen sowie die Dokumentation der Ergebnisse.
Hersteller müssen nachweisen:
- Eine vollständige chemische Charakterisierung
- Eine Bewertung von Extractables und Leachables
- Die Einhaltung der für die Klassifizierung des Produkts erforderlichen biologischen Endpunkte
- Einen wissenschaftlich begründeten biologischen Bewertungsbericht (BER)
Mit unseren Prüfdienstleistungen verfügen Hersteller über die Werkzeuge, um regulatorische Anforderungen effizient zu erfüllen und einen reibungslosen Weg zur Zertifizierung und Marktzulassung sicherzustellen.
ISO 11979-5 – Biokompatibilitätsanforderungen für ophthalmische Implantate
ISO 11979-5 ist die wichtigste internationale Norm für die Biokompatibilitätsprüfung von ophthalmischen Implantaten, einschließlich Intraokularlinsen (IOLs) und anderen implantierbaren Produkten, die in der Augenchirurgie eingesetzt werden. Da diese Produkte in direkten Kontakt mit hochsensiblen okulären Geweben kommen, definiert diese Norm spezifische Anforderungen an die biologische Sicherheit, die über den allgemeinen Rahmen der ISO 10993 hinausgehen.
Diese auf die Ophthalmologie ausgerichtete Norm stellt sicher, dass jedes Material und jede Komponente, die in einem intraokularen Implantat verwendet wird, für den langfristigen Einsatz im Auge als sicher nachgewiesen ist. ISO 11979-5 bietet detaillierte Leitlinien zur Bewertung von:
- Okulärer Reizung und intraokularer Reaktivität
- Zytotoxizität und systemischer Toxizität
- Extractables und Leachables spezifisch für intraokulare Exposition
- Langzeitkompatibilität im Auge
Durch die Einbeziehung dieser spezifischen Anforderungen unterstützt ISO 11979-5 Hersteller dabei, nachzuweisen, dass ihre ophthalmischen Produkte die höchsten Standards hinsichtlich Sicherheit, Reinheit, Materialstabilität und Biokompatibilität erfüllen. Diese Norm ist essenziell für regulatorische Einreichungen, Risikomanagementdokumentationen und die Marktzulassung von Intraokularlinsen und anderen ophthalmischen Implantaten.
ISO 10993-5 – Zytotoxizität
Der Zytotoxizitätstest für Medizinprodukte bewertet, ob Materialien oder deren Extrakte Zellschäden verursachen können, wenn sie mit lebenden Zellen in Kontakt kommen. Gemäß ISO 10993-5 umfasst die Biokompatibilitätsprüfung von Medizinprodukten In-vitro-Tests, bei denen kultivierte Zellen mit Produkt-Extrakten oder Materialien im direkten Kontakt exponiert werden, um potenziell schädliche auslaugbare Stoffe zu erkennen. Aufgrund seiner Schnelligkeit und Sensitivität ist dies häufig der erste Screening-Schritt im biologischen Bewertungsprozess.
ISO 10993-10 - Reizung und Hautsensibilisierung
ISO 10993-10 definiert die Biokompatibilitätsprüfung von Biomaterialien und Medizinprodukten mit Fokus auf dermale und mukosale Reaktionen, einschließlich Reizung, allergischer Reaktionen und Sensibilisierung. Diese Tests bewerten, ob das Medizinprodukt oder seine Bestandteile nach Kontakt mit Haut oder Schleimhaut entzündliche oder immunvermittelte Reaktionen auslösen können. Dies ist essenziell für Produkte mit direktem oder längerem Patientenkontakt, wie Verbände, Wearables, Implantate oder wiederverwendbare Instrumente.
ISO 10993-11 - Potenzielle systemische Toxizität von Medizinprodukten
Systemische Toxizitätsbewertungen prüfen, ob aus einem Medizinprodukt freigesetzte Chemikalien schädliche Wirkungen über den lokalen Anwendungsbereich hinaus verursachen können. Die Prüfung nach ISO 10993-11 umfasst akute, subakute und chronische systemische Toxizitätsendpunkte. Diese Biokompatibilitätsprüfungen für Medizinprodukte helfen, Risiken im Zusammenhang mit der Absorption, Verteilung, dem Metabolismus und der Ausscheidung potenziell gefährlicher Verbindungen zu identifizieren.Biokompatibilität
Anforderungen an die Prüfung von Medizinprodukten
Um globale regulatorische Anforderungen zu erfüllen, müssen Hersteller einem strukturierten, risikobasierten Ansatz gemäß ISO 10993-1 folgen. Abhängig von der Art des Produktkontakts (Oberfläche, Implantat, externe Kommunikation) und der Kontaktdauer (begrenzt, verlängert, langfristig) gelten unterschiedliche Anforderungen an die Biokompatibilität von Medizinprodukten.
Typische Anforderungen umfassen:
- Planung der biologischen Bewertung (BEP)
- Chemische Charakterisierung und toxikologische Risikobewertung (TRA)
- In-vitro- und In-vivo-Tests nach Bedarf
- Begründung für ausgelassene Tests
- Bewertung von Haltbarkeit und Alterung
- Bewertung der Auswirkungen von Herstellung und Sterilisation
- Abschließender biologischer Bewertungsbericht (BER)
Diese Anforderungen stellen sicher, dass das Produkt sicher ist, wie erwartet funktioniert und alle notwendigen Biokompatibilitätsstandards für den Marktzugang erfüllt.
Was sind die Vorteile der Biokompatibilitätsprüfung?
Die Prüfung der Biokompatibilität von Medizinprodukten ist eine wesentliche Dienstleistung, die wir durchführen, um die Sicherheit und Verträglichkeit dieser Produkte mit biologischen Systemen zu gewährleisten und letztlich die Gesundheit und das Wohlbefinden der Patienten zu schützen, die auf sie für medizinische Behandlungen und Versorgung angewiesen sind. Unter den zahlreichen Vorteilen dieser Prüfungen möchten wir besonders hervorheben:
Warum Applus+ Laboratories für Biokompatibilitätsprüfungen wählen?
Die Wahl von Applus+ Laboratories für Ihre Biokompatibilitätsbewertung bedeutet die Zusammenarbeit mit einem führenden Anbieter im Bereich der Prüfung von Medizinprodukten. Unsere Dienstleistungen, die den Anforderungen der FDA und den ISO-Normen entsprechen, sind speziell darauf ausgelegt, die strukturelle Integrität und Sicherheit Ihres Medizinprodukts zu gewährleisten
- Vollständig ausgestattetes modernes Labor mit neuesten Technologien
- Umfassende Expertise in der Materialbewertung
- Anerkannte und zertifizierte Labore und Mitarbeitende
Mit Aktivitäten in mehreren Ländern bietet Applus+ Laboratories seine fortschrittlichen Validierungs- und Prüfdienstleistungen weltweit an und gewährleistet den Zugang zu hochwertigen Testlösungen – unabhängig von Ihrem Standort.
Wir sind ein globales Unternehmen und erbringen unsere Prüfdienstleistungen weltweit, wobei wir allen unseren Kunden erstklassige Biokompatibilitätsprüfungen bieten.
Vertrauen Sie auf Applus+ Laboratories als Ihren zuverlässigen Partner für Biokompatibilitätsprüfungen. Wir stehen bereit, Sie mit unseren umfassenden Dienstleistungen und unserem Fachwissen zu unterstützen.