Chez Applus+ Laboratories, nous vous proposons des services d'essais sur les dispositifs médicaux, qui vous aident à améliorer le développement et l'évaluation de la conformité de vos dispositifs médicaux aux normes réglementaires ainsi que leur biocompatibilité, tout en vérifiant la sécurité de vos produits. Les essais de biocompatibilité sont inclus dans nos autres services d'essais de libération de lots :
Ces essais de biocompatibilité s’inscrivent dans le panel d’essai permettant la mise sur marché de votre dispositif:
- Validation du nettoyage
- Validation d'emballage
- Validation de la stabilité
- Caractérisation des matériaux et analyse chimique
Pourquoi les tests de biocompatibilité des dispositifs médicaux sont-ils importants ?
Les essais de biocompatibilité sur dispositifs médicaux sont essentiels pour garantir qu'aucun matériau, composant ou dispositif complet entrant en contact avec le corps humain ne provoque de réactions biologiques nocives. Grâce à ces essais, les fabricants peuvent évaluer si un dispositif est sûr, chimiquement stable et adapté à l'usage clinique auquel il est destiné. Ce processus est également essentiel pour démontrer la conformité réglementaire, car les agences internationales exigent une évaluation biologique complète dans le cadre de l'autorisation de mise sur le marché des dispositifs.
Les tests de biocompatibilité des dispositifs médicaux évaluent les interactions entre les matériaux des dispositifs et les systèmes biologiques, afin de garantir que le dispositif ne provoque pas d'effets cytotoxiques, irritants, sensibilisants ou toxiques systémiques. Ces évaluations constituent un élément fondamental de la gestion des risques et de la sécurité des patients.
La caractérisation chimique comprend plusieurs parties de la norme ISO 10993 :
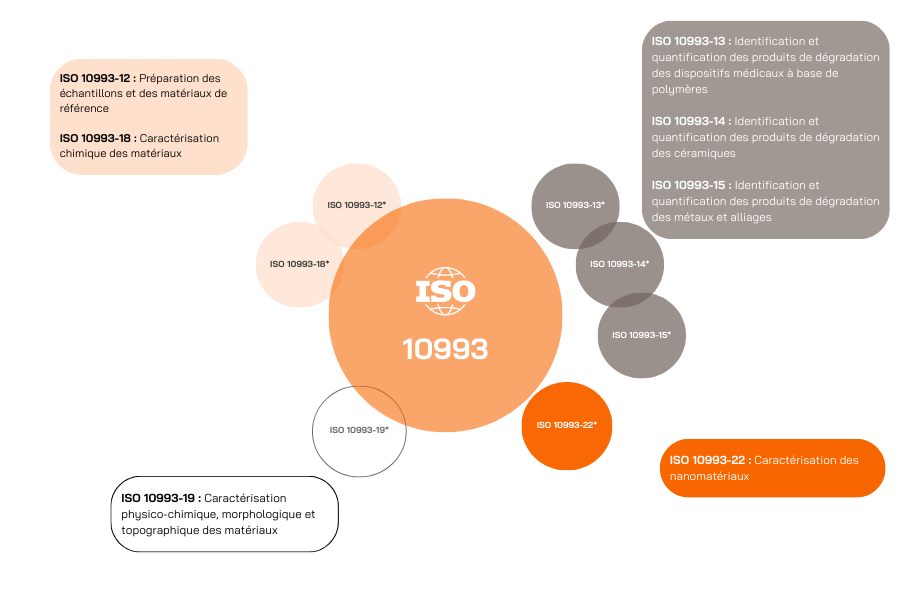
Les lignes directrices pour réaliser l’évaluation de la biocompatibilité se trouvent dans la norme ISO 10993-1 et indiquent les essais à effectuer selon le type de dispositif, la durée du contact et la nature du contact avec le corps.
Une attention particulière doit être portée au potentiel du matériau à libérer des composés (associé au procédé de fabrication ou à la dégradation du matériau à son stade initial et après vieillissement) afin de valider la date de péremption.
Caractérisation Chimique et Essais d’Extractibles et Relargables
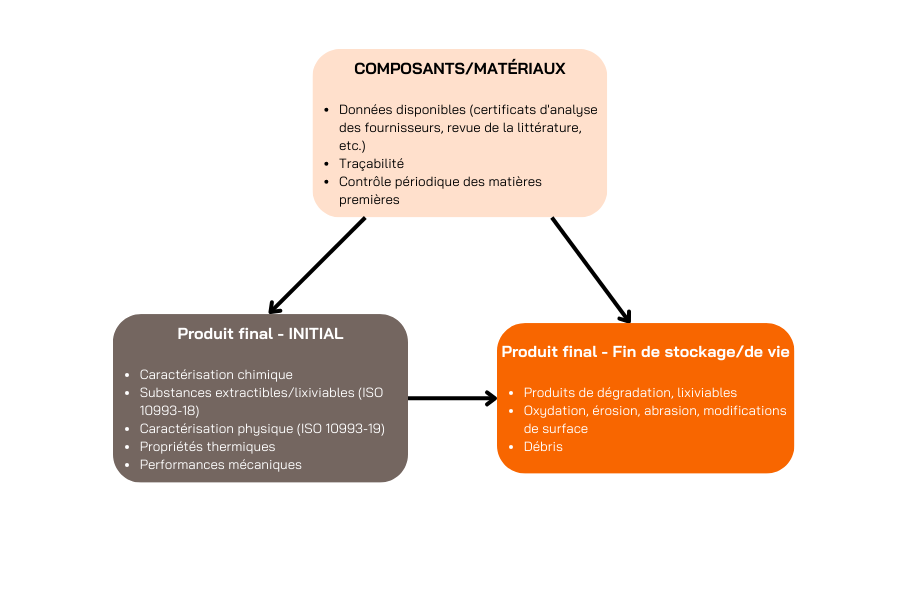
Il est important de caractériser le matériau dès le stade initial afin de déterminer le niveau de risque et d'identifier les composés chimiques ou les produits non contrôlés susceptibles d'avoir une incidence sur la sécurité globale des dispositifs. Cette caractérisation constitue la toute première étape de l'élaboration de la stratégie et des exigences en matière d'évaluation biologique.
La détermination des caractéristiques chimiques après vieillissement et l'étude de l'interaction entre le dispositif médical et son emballage sont tout aussi importantes pour établir la durée de conservation et déterminer la date de péremption.
Analyses Physico-Chimiques Selon l'ISO 10993-12 et l'ISO 10993-18
Cette analyse initiale est axée sur l’étude des propriétés physiques et chimiques des matériaux utilisés dans les dispositifs médicaux.
Tous les échantillons de dispositifs médicaux sont extraits conformément aux exigences d’ISO 10993-12 (en fonction de la nature du contact, de la durée, du marché visé et de la nature chimique du dispositif).
La norme ISO 10993-18 fournit des lignes directrices pour identifier et quantifier les substances chimiques susceptibles d’être libérées par le matériau du dispositif médical (extractibles et lixiviables), ainsi que pour analyser sa composition chimique et sa structure.
- Analyse des composés volatils (COV) tels que les solvants résiduels (terpénoïdes) et les alcools par chromatographie en phase gazeuse headspace (HS-GC-MS)
- Analyse des composés semi-volatils (SVOC), par exemple les monomères résiduels et additifs de faible masse molaire (alcanes, alcools, esters, siloxanes, etc.) via chromatographie en phase gazeuse (GC-MS)
- Analyse des composés non volatils (NVOC), tels que les additifs de fabrication et matériaux de poids moléculaire élevé, via chromatographie liquide (LC-MS)
- Analyse des composés minéraux et inorganiques via ICP-OES et ICP-MS
- Analyse des composés ioniques (phosphate, chlorate, nitrate, bromure, etc.) via chromatographie ionique (IC)
Caractérisation Physico-Chimique, Morphologique et Topographique des Matériaux selon la norme ISO 10993-19
En plus de ces évaluations obligatoires, une caractérisation chimique supplémentaire peut être réalisée pour mieux caractériser vos dispositifs médicaux (FTIR, MEB, DSC, SEC). Vous trouverez plus de détails dans la section dédiée à la caractérisation chimique.
Élément essentiel de l’évaluation biologique des dispositifs médicaux, ce processus implique une analyse approfondie des propriétés physiques, chimiques et de surface des matériaux utilisés afin de garantir leur sûreté, leurs performances et leur biocompatibilité. La compréhension de ces propriétés vous aide à prévoir comment le matériau interagit avec les systèmes biologiques.
La norme ISO 10993-19 couvre de nombreux aspects, de l’analyse de la composition élémentaire et moléculaire du matériau à ses propriétés thermiques, en passant par la structure et la morphologie de sa surface, ainsi que sa mouillabilité ou hydrophobie.
Analyse des produits de dégradation (ISO 10993-13/14/15)
Un autre aspect crucial consiste à contrôler l’évolution du dispositif au fil du temps.
Des produits de dégradation ou résidus de fabrication non contrôlés doivent être vérifiés afin d’assurer la sécurité à long terme des dispositifs, aussi bien dans des conditions de stockage que lors de l’utilisation en conditions réelles.
Grâce à ce processus, nous pouvons comprendre la stabilité et la sûreté à long terme des dispositifs médicaux à base de polymères, en identifiant et quantifiant tout sous-produit libéré à mesure que le matériau se dégrade au fil du temps.
Dans ce volet de la biocompatibilité, des essais de stabilité sont réalisés, ainsi que des essais similaires à ceux décrits dans ISO 10993-18, mais après vieillissement. Pour les implants métalliques, la résistance à la corrosion et la libération de métal peuvent être évaluées.
Accompagnement en Matière de Conformité Réglementaire pour les Tests de Biocompatibilité des Dispositifs Médicaux
La démonstration de la conformité aux réglementations internationales constitue un élément essentiel des essais de biocompatibilité des dispositifs médicaux. Les organismes de réglementation tels que la FDA (États-Unis), le MDR (Union européenne) et d'autres agences internationales exigent une évaluation biologique exhaustive conforme à la norme ISO 10993-1. Les essais de biocompatibilité des dispositifs médicaux comprennent l'évaluation des risques, la sélection des essais biologiques appropriés, la justification des dérogations aux essais et la documentation des résultats.
Les fabricants doivent fournir :
- Une caractérisation chimique complète
- Une évaluation des substances extractibles et relargables
- La conformité aux critères biologiques requis pour la classification du dispositif
- Un rapport d'évaluation biologique (BER) scientifiquement fondé
Grâce à nos services d'essais, les fabricants disposent des outils nécessaires pour répondre efficacement aux exigences réglementaires, ce qui leur garantit un parcours sans encombre vers la certification et l'autorisation de mise sur le marché.
ISO 11979-5 – Exigences de Biocompatibilité pour les Implants Ophtalmiques
La norme ISO 11979-5 est la principale norme internationale régissant les essais de biocompatibilité des implants ophtalmiques, notamment les lentilles intraoculaires (LIO) et autres dispositifs implantables utilisés en chirurgie ophtalmologique. Étant donné que ces produits entrent en contact direct avec des tissus oculaires extrêmement sensibles, cette norme définit des exigences spécifiques en matière de sécurité biologique qui vont au-delà du cadre général de la norme ISO 10993.
Cette norme spécifique à l'ophtalmologie garantit que tous les matériaux et composants utilisés dans un implant intraoculaire ont fait l'objet de tests prouvant leur innocuité pour une utilisation à long terme à l'intérieur de l'œil. La norme ISO 11979-5 fournit des recommandations détaillées pour l'évaluation :
- Irritation oculaire et réactivité intraoculaire
- Cytotoxicité et toxicité systémique
- Substances extractibles et relargables spécifiques à l'exposition intraoculaire
- Compatibilité oculaire à long terme
En intégrant ces exigences spécifiques, la norme ISO 11979-5 aide les fabricants à démontrer que leurs dispositifs ophtalmiques répondent aux normes les plus strictes en matière de sécurité, de pureté, de stabilité des matériaux et de biocompatibilité. Cette norme est indispensable pour les dossiers réglementaires, la documentation relative à la gestion des risques et l'autorisation de mise sur le marché des lentilles intraoculaires et autres implants ophtalmiques.
ISO 10993-5 – Cytotoxicité
Le test de cytotoxicité des dispositifs médicaux permet de déterminer si les matériaux ou leurs composés extractibles peuvent provoquer la mort cellulaire lorsqu'ils entrent en contact avec des cellules vivantes. Conformément à la norme ISO 10993-5, les essais de biocompatibilité des dispositifs médicaux comprennent des tests in vitro consistant à exposer des cellules en culture à des extraits du dispositif ou à des matériaux en contact direct, afin de détecter les composés relargables potentiellement nocifs. En raison de sa rapidité et de sa sensibilité, ce test constitue souvent la première étape de dépistage dans le processus d'évaluation biologique.
ISO 10993-10 - Irritation et Sensibilisation Cutanée
La norme ISO 10993-10 définit les essais de biocompatibilité des biomatériaux et des dispositifs médicaux, en mettant l'accent sur les réactions cutanées et muqueuses, notamment l'irritation, les réactions allergiques et la sensibilisation. Ces essais permettent de déterminer si le dispositif médical ou ses composants sont susceptibles de provoquer des réactions inflammatoires ou à médiation immunitaire après un contact avec la peau ou les muqueuses. Cela est essentiel pour les dispositifs en contact direct ou prolongé avec le patient, tels que les pansements, les dispositifs portables, les implants ou les instruments réutilisables.
ISO 10993-11 - Toxicité Systémique Potentielle des Dispositifs Médicaux
Les évaluations de la toxicité systémique visent à déterminer si les substances chimiques libérées par un dispositif médical peuvent produire des effets nocifs au-delà de la zone d'application locale. Les essais prévus par la norme ISO 10993-11 portent sur les paramètres de toxicité systémique aiguë, subaiguë et chronique. Ces essais de biocompatibilité des dispositifs médicaux permettent d'identifier les risques liés à l'absorption, à la distribution, au métabolisme et à l'excrétion de composés potentiellement dangereux.
Exigences en Matière d'Essais des Dispositifs Médicaux
Pour répondre aux exigences réglementaires internationales, les fabricants doivent suivre une approche structurée et fondée sur les risques, telle que définie par la norme ISO 10993-1. En fonction de la nature du contact avec le dispositif (surface, implant, communication externe) et de la durée de ce contact (limité, prolongé, à long terme), différentes exigences de biocompatibilité s'appliquent aux dispositifs médicaux.
Les exigences habituelles incluent :
- Planification de l'évaluation biologique (BEP)
- Caractérisation chimique et évaluation des risques toxicologiques (TRA)
- Essais in vitro et in vivo selon les besoins
- Justification des essais omis
- Évaluations de la durée de conservation et du vieillissement
- Évaluation des effets liés à la fabrication et à la stérilisation
- Rapport final d'évaluation biologique (BER)
Ces exigences garantissent que le dispositif est sûr, qu'il fonctionne comme prévu et qu'il respecte toutes les normes de biocompatibilité requises pour sa mise sur le marché.
Pourquoi choisir Applus+ Laboratories pour les Essais de Biocompatibilité ?
En choisissant Applus+ Laboratories pour votre évaluation de biocompatibilité, vous faites appel à un leader reconnu dans le domaine des essais de dispositifs médicaux. Nos services, conformes aux exigences de la FDA et aux normes ISO, sont spécialement conçus pour garantir l'intégrité structurelle et la sécurité de votre dispositif médical
- Laboratoire dernier cri entièrement équipé et doté des dernières technologies
- Solide expertise en matière d'évaluation des matériaux
- Laboratoires et collaborateurs reconnus et certifiés
Présent dans de nombreux pays, Applus+ Laboratories propose ses services de pointe en matière de tests de validation des emballages à des clients du monde entier, garantissant ainsi l'accès à des solutions de test de qualité supérieure, où que vous soyez.
En tant qu'entreprise internationale, nous proposons nos services d'essais partout dans le monde, offrant à tous nos clients des essais de biocompatibilité de très haut niveau.
Faites confiance à Applus+ Laboratories: votre partenaire de confiance pour les essais de biocompatibilité. Nous sommes à votre disposition pour vous accompagner dans vos projets grâce à notre large gamme de services et à l'expertise de nos spécialistes.