En Applus+ Laboratories podemos ofrecerle nuestros excelentes ensayos de dispositivos médicos, que le ayudan a mejorar el desarrollo y la evaluación de conformidad con las normas regulatorias de sus dispositivos médicos y su biocompatibilidad, al mismo tiempo que se verifica la seguridad de sus productos. El ensayo de biocompatibilidad se incluye con nuestros otros ensayos de liberación de lote:
- Validación de limpieza de dispositivos médicos
- Enayo del envasado de dispositivos médicos
- Ensayo de estabilidad de dispositivos médicos
- Caracterización y química para dispositivos médicos
¿Por qué son Importantes los Ensayos de Biocompatibilidad para los Dispositivos Médicos?
Los ensayos de biocompatibilidad para dispositivos médicos son esenciales para garantizar que cualquier material, componente o dispositivo final que entre en contacto con el cuerpo humano no desencadene respuestas biológicas perjudiciales. A través de los ensayos de biocompatibilidad, los fabricantes pueden evaluar si un dispositivo es seguro, químicamente estable y adecuado para su uso clínico previsto. Este proceso es también fundamental para demostrar el cumplimiento normativo, ya que los organismos reguladores exigen una evaluación biológica completa como parte de la aprobación del dispositivo.
Los ensayos de biocompatibilidad de dispositivos médicos evalúan las interacciones entre los materiales del dispositivo y los sistemas biológicos, asegurando que el dispositivo no produzca efectos citotóxicos, irritantes, sensibilizantes o tóxicos sistémicos. Estas evaluaciones constituyen un componente básico de la gestión de riesgos y de la seguridad del paciente.
La caracterización química incluye varias partes de la Norma ISO 10993:
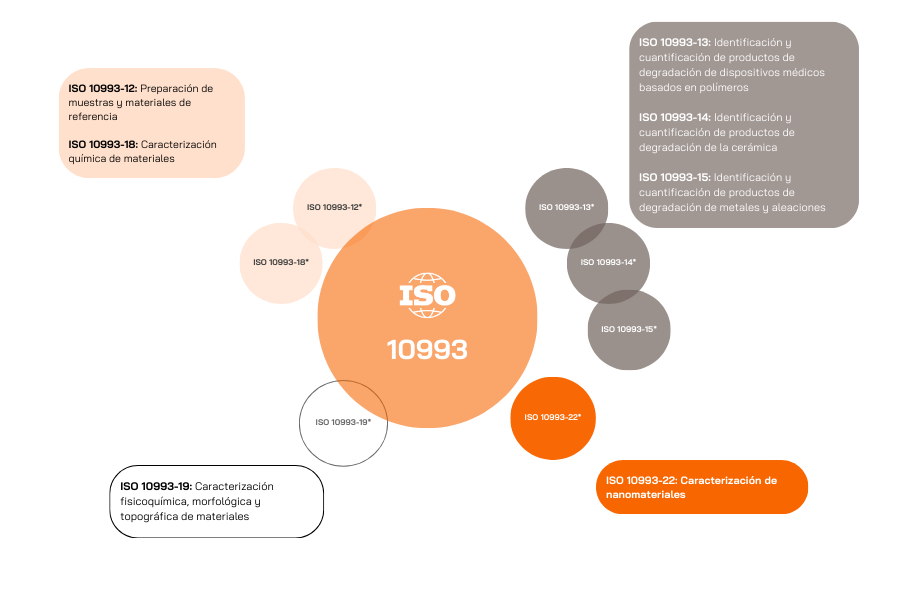
Las directrices para realizar la evaluación de la biocompatibilidad se pueden encontrar en la Norma ISO 10993-1 y proporcionan los ensayos requeridos a realizar según el tipo de dispositivo, la duración del contacto y la naturaleza del contacto con el cuerpo.
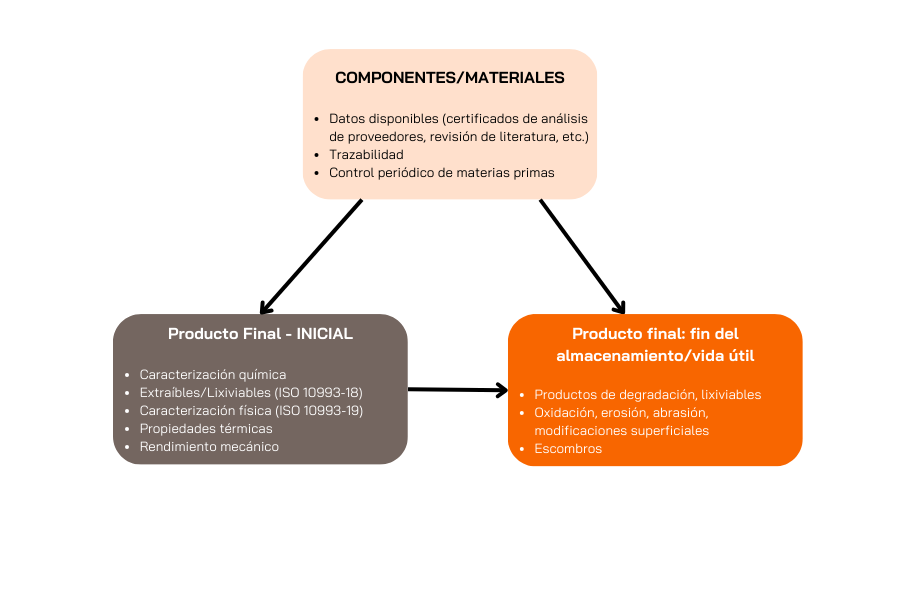
Se requiere especial atención al potencial del material para liberar compuestos (asociados al proceso de fabricación, o a la degradación del material en su etapa inicial y tras el envejecimiento para validar la fecha de caducidad.
Caracterización Química y Ensayos de Sustancias Extraíbles y Lixiviables
Caracterizar el material en su etapa inicial es importante para determinar el nivel de riesgo y la liberación de compuestos químicos o productos no controlados que podrían impactar la seguridad general de los dispositivos. Esta caracterización es el primer paso en la elaboración de la estrategia y los requerimientos de evaluación biológica.
La determinación de la caracterización química tras el envejecimiento y la interacción del dispositivo médico con su envasado es igualmente importante para establecer la vida útil y determinar la fecha de caducidad.
Análisis físico-químicos según la Norma ISO 10993-12
Este análisis inicial se centra en estudiar las propiedades físicas y químicas de los materiales utilizados en dispositivos médicos.
Todas las muestras de dispositivos médicos se extraen de acuerdo con los requisitos de la Norma ISO 10993-12 (dependiendo de la naturaleza del contacto, la duración, el mercado objetivo y la naturaleza química del dispositivo).
La Norma ISO 10993-18 proporciona orientación sobre la identificación y cuantificación de sustancias químicas que podrían liberarse potencialmente del material del dispositivo médico, sustancias extraíbles y lixiviables, la composición química del material y su estructura química.
- Análisis de compuestos volátiles (VOC) como solvente residual (terpenoide) y alcoholes mediante cromatografía de cabeza (HS-GC-MS)
- Análisis de compuestos semivolátiles (SVOC) como monómero residual y aditivos de bajo peso (alcanos, alcoholes, ésteres, siloxanos…) mediante cromatografía de gases (GC-MS)
- Análisis de compuestos no volátiles (NVOC) como aditivos de fabricación y de materiales (aditivo de alto peso) mediante cromatografía líquida (LC-MS)
- Análisis de compuestos minerales e inorgánicos mediante ICP-OES e ICP-MS
- Análisis de compuestos iónicos (fosfato, clorato, nitrato, bromuro,…) mediante cromatografía iónica (CI)
Caracterización fisicoquímica, morfológica y topográfica de materiales según la Norma ISO 10993-19
Además de estas evaluaciones obligatorias, se podría realizar una caracterización química adicional para caracterizar mejor sus dispositivos médicos (FTIR, SEM, DSC, SEC). Más detalles en la caracterización química.
Parte esencial de la evaluación biológica de los dispositivos médicos, este proceso implica un análisis integral de las propiedades físicas, químicas y superficiales de los materiales utilizados en dispositivos médicos para garantizar su seguridad, rendimiento y biocompatibilidad. Comprender estas propiedades le ayudará a predecir cómo interactuará el material con los sistemas biológicos.
La Norma ISO 10993-19 abarca muchas dimensiones diferentes, desde el análisis de la composición elemental y molecular de los materiales hasta sus propiedades térmicas, la estructura y morfología de la superficie o la humectabilidad y la hidrofobicidad de la misma.
Análisis de productos de degradación (ISO 10993-13/14/15)
Otro aspecto crucial es controlar la evolución del dispositivo a lo largo del tiempo.
Los subproductos de degradación y los productos resultantes de la fabricación no controlados son, en última instancia, algo que se debe verificar para asegurar la seguridad a largo plazo de los dispositivos, tanto en condiciones de almacenamiento como en condiciones de uso.
A través de este proceso, podemos entender la estabilidad y seguridad a largo plazo de los dispositivos médicos basados en polímeros, identificando y cuantificando cualquier subproducto liberado a medida que el material se descompone con el tiempo.
En esta parte de la biocompatibilidad, se realiza el ensayo de estabilidad y se efectúan ensayos similares a los de la Norma ISO 10993-18 después del envejecimiento. Se podría evaluar la resistencia a la corrosión y la lixiviación metálica en implantes metálicos.
Asistencia para el Cumplimiento Regulatorio en los Ensayos de Biocompatibilidad
Demostrar el cumplimiento de las normativas internacionales es una parte crítica de los ensayos de biocompatibilidad de los dispositivos médicos. Organismos como la FDA (Estados Unidos), el MDR (Unión Europea) y otros reguladores internacionales exigen una evaluación biológica completa alineada con la ISO 10993 1. Los requisitos de ensayos de biocompatibilidad incluyen la evaluación de riesgos, la selección de los ensayos biológicos apropiados, la justificación de excepciones y la documentación de resultados.
- Los fabricantes deben demostrar:
- Una caracterización química completa
- Una evaluación de extractables y lixiviables
- El cumplimiento de los endpoints biológicos requeridos para la clasificación del dispositivo
- Un informe de evaluación biológica (BER) científicamente justificado
Con nuestros servicios de ensayos, los fabricantes disponen de herramientas para navegar eficazmente por las expectativas regulatorias, garantizando un proceso fluido hacia la certificación y aprobación de mercado.
ISO 11979 5 – Requisitos de Biocompatibilidad para Implantes Oftálmicos
La ISO 11979 5 es la norma internacional clave que regula los ensayos de biocompatibilidad de implantes oftálmicos, incluidas las lentes intraoculares (IOL) y otros dispositivos implantables utilizados en cirugía ocular. Como estos productos entran en contacto directo con tejidos oculares altamente sensibles, esta norma define requisitos específicos que van más allá del marco general de la ISO 10993.
Esta norma centrada en oftalmología garantiza que todo material o componente utilizado en un implante intraocular sea seguro para su uso prolongado dentro del ojo. La ISO 11979 5 proporciona directrices detalladas para evaluar:
- Irritación ocular y reactividad intraocular
- Citotoxicidad y toxicidad sistémica
- Extractables y lixiviables específicos de la exposición intraocular
- Compatibilidad ocular a largo plazo
ISO 10993 5 – Citotoxicidad
El ensayo de citotoxicidad evalúa si los materiales o sus extractables pueden causar muerte celular al entrar en contacto con células vivas. Según la ISO 10993 5, los ensayos de biocompatibilidad incluyen ensayos in vitro que exponen cultivos celulares a extractos del dispositivo o a materiales en contacto directo, para detectar lixiviables potencialmente dañinos. Suele ser el primer paso de cribado por su rapidez y sensibilidad.
ISO 10993 10 – Irritación y Sensibilización Cutánea
La ISO 10993 10 define los ensayos de biocompatibilidad centrados en respuestas dérmicas y mucosas, como irritación, reacciones alérgicas y sensibilización. Estos ensayos evalúan si el dispositivo o sus componentes pueden desencadenar respuestas inflamatorias o mediadas por el sistema inmunitario tras el contacto con piel o mucosas.
ISO 10993 11 – Toxicidad Sistémica Potencial
Las evaluaciones de toxicidad sistémica determinan si los químicos liberados por un dispositivo pueden producir efectos nocivos más allá del área de aplicación. La ISO 10993 11 incluye endpoints de toxicidad aguda, subaguda y crónica. Estos ensayos ayudan a identificar riesgos relacionados con absorción, distribución, metabolismo y excreción de compuestos potencialmente peligrosos.
Requisitos de los Ensayos de Biocompatibilidad para Dispositivos Médicos
Para cumplir con los requisitos regulatorios globales, los fabricantes deben seguir un enfoque estructurado basado en riesgos definido por la ISO 10993 1. Según la naturaleza del contacto (superficie, implante, comunicación externa) y la duración (limitado, prolongado o largo plazo), se aplican distintos requisitos.
Requisitos típicos:
- Plan de evaluación biológica (BEP)
- Caracterización química y evaluación toxicológica del riesgo (TRA)
- Ensayos in vitro e in vivo según necesidad
- Justificación de ensayos omitidos
- Evaluación de vida útil y envejecimiento
- Evaluación del impacto de fabricación y esterilización
- Informe final de evaluación biológica (BER)
¿Por qué elegir Applus+ Laboratories para el ensayo de biocompatibilidad?
Elegir Applus+ Laboratories para su evaluación de biocompatibilidad lo alinea con un líder distinguido en el ensayo de dispositivos médicos. Nuestros servicios, conformes con los requisitos de la FDA y las normas ISO, están diseñados específicamente para garantizar la integridad estructural y la seguridad de su dispositivo médico.
- Laboratorio totalmente equipado y moderno con las últimas tecnologías
- Amplia experiencia y habilidades en la evaluación de materiales
- Laboratorios y empleados reconocidos y certificados
Con operaciones en varios países, Applus+ Laboratories lleva nuestros servicios de validación de envasado de vanguardia a clientes en todo el mundo, garantizando el acceso a soluciones de ensayo superiores dondequiera que se encuentren.
Somos una empresa global y, por lo tanto, ofrecemos nuestros servicios de ensayo en cualquier parte del mundo, proporcionando ensayos de biocompatibilidad de primer nivel a todos nuestros clientes.
Confíe en Applus+ Laboratories como su socio de confianza para el ensayo de biocompatibilidad. Estamos listos para apoyar sus esfuerzos con nuestros amplios servicios y conocimientos expertos.